摘要:通过有机催化靛红衍生的3-甲基吲哚醇和3-甲基-2吲哚烯烃发生不对称的[3+2]环加成反应。反应构建了有高度立体选择性的氧化吲哚螺吲哚并环戊烷骨架(产率:72-99%, >95:5 dr, ee: 90-98%)。这个骨架具有连续三个手性中心,并且产生一个季碳中心。26553
毕业论文关键词:有机催化、对映选择性、不对称合成
Chiral phosphoric acid catalytic asymmetric Construction of indole - cyclopentane via Catalytic Asymmetric Formal [3+2] Cycloadditions
Abstract: We use isatin-derived 3-indolylmethanol and 3-methyl-2-vinylindole built an organocatalytic asymmetric formal [3+2] cycloaddition, leading to a highly stereoselective construction of spiro[cyclopenta[b]indole-1,3'-oxindole] (72-99% yield, all >95:5 dr, 90-98% ee), which have three contiguous stereogenic centers, one of which is an all-carbon quaternary stereogenic center.
Keyword: Organic catalysis; Enantioselectivity; Asymmetric synthesis
1 前言
光学纯的3’3-螺氧化吲哚骨架和环戊醇吲哚骨架是构成1和合成2许多天然生物碱的化合物,具有良好的药理活性,如抗癌3、SIRT 1的抑制剂4、受体雄性激素受体选择性的调节器5(Figure 1)。因此,手性3’3-螺氧化吲哚骨架和环戊醇吲哚骨架的合成引起了高度的重视,这两类骨架启发了我们设想用这两个化合物构建一个新的氧化吲哚螺吲哚并环戊烷骨架,这个骨架可能增强其重要的生物活性2(Scheme 1)。
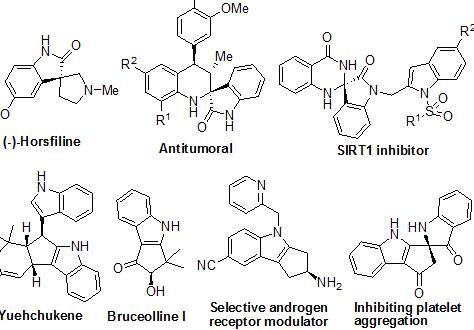
Figure1: 包含手性3’3-螺氧化吲哚和环戊醇吲哚骨架的活性分子
Scheme 1. 氧化吲哚螺吲哚并环戊烷骨架的设计
催化不对称[3+2]环加成反应是构建五元环是一种可靠的方法6。通常1,3 - 偶极子作为合成子催化不对称[3+2]环加成反应的深入研究,建立了良好的五元手性杂环化合物,如叠氮化物,甲亚胺亚胺,硝酮,亚甲胺叶立德,(硫代)羰基内鎓盐,腈氧化物等6。与此相反,其他类型3C合成子不对称催化的非1,3 - 偶极[3+2]环加成利用其他类型的不完善,只有有限的例子,其采用I-V 中的底物代替1,3-偶极子(Scheme 2)7。
Scheme 2. 催化不对称[3+2]环加成反应研究进展
2 实验部分
2.1 仪器及试剂
高效液相色谱仪 Bruker AV400 MHz型核磁共振仪,旋转蒸发仪,红外光谱仪,靛红,溴苄,吲哚,石油醚,乙酸乙酯,正己烷,异丙醇,氘代氯仿,氯仿(所用试剂均为市售分析纯)。
2.2 反应的提出与设计:
近日,3-甲基吲哚醇(VI,in Scheme 3)作为一种活性试剂在有机合成中显示出巨大潜力,用于多种具有对映选择性的亲核取代的反应8-9。然而3-甲基吲哚醇很少被用作像3C中的合成子参与催化不对称环加成反应,特别是有对映体选择性的[3+2]环加成反应。更重要的是,这种转变提供了一种有效的构建手性氧化吲哚并环戊烷骨架的策略。
Scheme 3. 3-甲基官能团化吲哚醇参与的不对称反应研究
为此,我们想知道3-甲基-2-吲哚烯是否可以作为一个合适的烯烃组分与靛红衍生的3-甲基吲哚醇进行不对称形式[3+2]环加成反应,这将建立手性氧化吲哚螺吲哚并环戊烷骨架骨架的另一个吲哚基团(Scheme 4)。在我们以前的不对称催化反应的成功的基础上9c-d,10,我们在此提出催化有机不对称正式[3+2]环加成中的手性磷酸(CPA)的存在11,导致高度立体选择性构建氧化吲哚螺吲哚并环戊烷骨架(产率:72-99%, >95:5 dr, ee: 90-98%)。
Scheme 4. 氧化吲哚螺吲哚并环戊烷骨架的设计
2.3 结果与讨论
2.3.1 条件的筛选: 手性磷酸催化的不对称形式[3+2]环加成反应构建吲哚并环戊烷骨架:http://www.751com.cn/huaxue/lunwen_20778.html

