1.2锂离子电池简介
1.2.1锂离子电池的工作原理
众所周知锂离子电池作为一种电能-化学能互相转化的电池,其主要由三部分组成:电极材料(包括正极材料和负极材料)、电解液、隔膜。电极材料是电池主要的储能介质,其组成元素为可逆的脱嵌锂离子的化合物。电解液是锂盐的重要运载体,在电池的内部起到离子导电的功能,锂离子主要集中在这里。位于正负极材料当中的是隔膜,隔膜能进行离子与离子间的传输并阻隔电子导电,防止正负极间发生短路。图1-1为锂离子电池的基本工作原理。
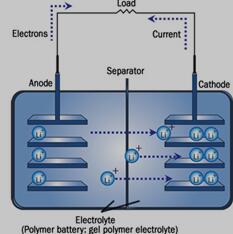
图1-1锂离子电池的工作原理
当电池充电时,Li+离子从正极脱嵌出,由经电解质溶液再通过隔膜嵌入负极中,此时正极中的活性物质处于贫锂状态;反之,当电池放电时,Li+离子则从负极中脱出,通过电解质溶液和隔膜再嵌入到正极中,正极活性物为富锂状态。为保持电荷平衡,当充放电时,会有一大部分的电子经过外电路而传递,和Li+离子会和后一起在正、负极之间来回迁移,让正、负极产生相应的氧化还原反应,并保持相对的电位。嵌入和脱出会引起电池材料层间距离的改变,但绝大多数的情况下是不会对材料晶体结构的变化有任何影响的,因此锂离子电池具有良好的安全性和循环稳定性。这也是我们要探究锂离子电池的主要原因,而构成正、负极的嵌锂化合物的化学性质、导致Li+离子浓度的最主要原因是工作电位的大小[6]。
我们可以从锂离子电池的工作原理中可以看到,锂离子电池的本质上是一个 Li+离子浓差电池,组成正负电极的是两种不同的锂离子嵌入化合物。 锻烧条件对富锂正极材料Li2MnO3-LiMO2电化学性能的影响研究(3):http://www.751com.cn/cailiao/lunwen_28371.html

